ЛМ11А-31 лек успорава напредовање Алцхајмерове болести у испитивању
Последње прегледано: 14.06.2024

Сви иЛиве садржаји су медицински прегледани или проверени како би се осигурала што већа тачност.
Имамо стриктне смјернице за набавку и само линкамо на угледне медијске странице, академске истраживачке институције и, кад год је то могуће, медицински прегледане студије. Имајте на уму да су бројеви у заградама ([1], [2], итд.) Везе које се могу кликнути на ове студије.
Ако сматрате да је било који од наших садржаја нетачан, застарио или на неки други начин упитан, одаберите га и притисните Цтрл + Ентер.

У недавној студији објављеној у Натуре Медицине, истраживачи су спровели рандомизовано, двоструко слепо, плацебом контролисано испитивање фазе 2а како би испитали безбедност и ефикасност ЛМ11А-31 у лечењу Алцхајмерове болести (АД) кроз модулација рецептора неуротрофина п75 (п75НТР).
АД са касним почетком је најчешћи облик деменције, коју карактерише синаптичка инсуфицијенција, дегенерација и губитак нервних ћелија. Иако два главна лека за лечење АД циљају на акумулацију абнормалног амилоид-β или тау протеина, они се баве само делом патофизиологије. Други приступ је циљање рецептора и сигналних мрежа које утичу на основне биолошке путеве. Претклиничке студије показују да модулација п75НТР са новим малим молекулом ЛМ11А-31 смањује синаптички губитак изазван амилоидом и патолошким тау.
Опис студије
У овом рандомизованом клиничком испитивању, истраживачи су испитали да ли ЛМ11А-31 може да успори напредовање Алцхајмерове болести модулацијом п75НТР код људи.
Учесницима студије су даване оралне капсуле ЛМ11А-31 у дозама од 200 мг и 400 мг или плацебо у односу 1:1:1 за 242 пацијента са благом до умереном астмом током 26 недеља. Учесници су имали биолошки потврђену Алцхајмерову болест (ниво амилоида β протеина 42 (Аβ42) цереброспиналне течности испод 550 нг/Л или однос Аβ42:β40 испод 0,89), дијагностиковану према МцКханн критеријумима, са Мини Псицхиатриц СЕ (ММСЕ) скором од 26 Скала геријатријске депресије (ГДС) има мање од 5,0, модификована Хацински исхемијска скала (ХИС) резултати ≤ 4,0, формално образовање ≥ 8 година и претходни когнитивни пад ≥ 6 месеци.
Учесници који испуњавају услове су узимали инхибиторе ацетилхолинестеразе (АЦхЕИ) или парцијалне антагонисте НМДА рецептора ≥ 3 месеца пре уласка у студију. Нису узимали недозвољене лекове као што су антипсихотици, бензодиазепини, антиепилептички лекови, седативи, централно активни антихипертензиви, ноотропици (осим гинко билобе) или аналгетици који садрже опиоиде.
Примарни исход студије била је безбедност и подношљивост лека према процени Цолумбиа Суицидал Идеатион анд Бехавиор Северити Ратинг Сцале (Ц-ССРС), витални знаци, крвни притисак и хематолошки параметри. За процену секундарних когнитивних исхода коришћени су биомаркери структурне магнетне резонанце (сМРИ), позитронска емисиона томографија флуородеоксиглукозе (ФДГ-ПЕТ) и биомаркери цереброспиналне течности (ЦСФ). АД индикатори су укључивали тау фосфорилисан на Тхр181, укупни тау протеин, Аβ40, Аβ42 и АЦхЕ активност. Тим је користио индивидуализовани неуропсихолошки тест за процену секундарних когнитивних исхода на почетку, 12. И 26. Недеље.
Резултати истраживања
Студија је открила да је ЛМ11А-31 безбедан и да се добро толерише, без значајних забринутости за безбедност. Најчешћи нежељени ефекти укључивали су главобољу, дијареју, еозинофилију и назофарингитис, при чему су гастроинтестинални проблеми и еозинофилија главни разлози за укидање лека. Било је више прекида у групи од 400 мг у поређењу са 200 мг и плацебо групама. МРИ није открио никакве забринутости за безбедност лекова, укључујући абнормалности везане за амилоид. Није било значајних разлика у когнитивним резултатима или амилоидним абнормалностима између две третиране групе.
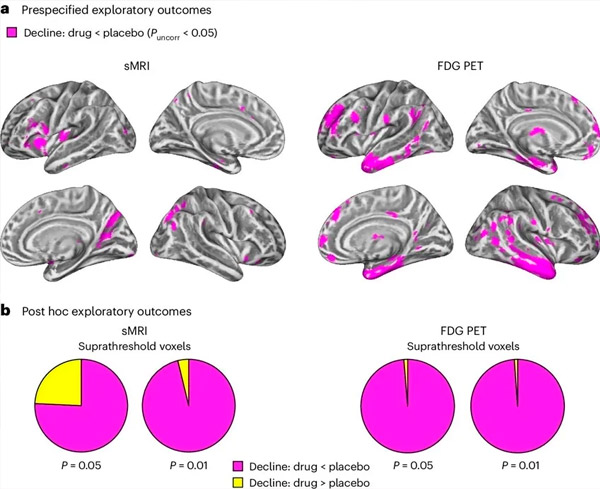
А. Двофакторска анализа мешовитих модела коваријансе је испитивала интеракције између третмана (лек или плацебо) и времена (пре или после третмана). Једносмерни т-контраст који испитује хипотезу интеракције (лек успорава напредовање у поређењу са плацебом) показао је да третман ЛМ11А-31 успорава лонгитудиналну дегенерацију (леви панели) и хипометаболизам глукозе (десни панели) у групи која је лечена леком (цМРИ, н = 127 ПЕТ, н = 121), у поређењу са плацебо групом (сМРИ, н = 66; ПЕТ, н = 62). Воксели који показују ову интеракцију су приказани на некоригованом прагу П &лт; 0,05 (магента боја) на површини кортекса специфичној за популацију. Лева и десна хемисфера су приказане у горњем и доњем реду. Региони мозга који показују интеракције које нису у складу са хипотезом приказани су на слици 7 у додатним подацима.
б. Укупан број воксела у унапред дефинисаним рањивим АД регионима мозга (укупна површина кружних дијаграма) који показују или интеракцију конзистентну хипотезу (магентна боја) или интеракцију недоследну хипотезу (жута боја) у сваком од модалитета снимања (цМРИ, леви панел; ФДГ ПЕТ, десни панел) на све либералнијим неприлагођеним П праговима &лт; 0,01 и П &лт; 0.05. Монте Карло симулације су показале да су односи воксела који показују ефекте који су у складу са хипотезом у односу на оне који нису у складу са хипотезом били значајно већи од оних уочених из насумично генерисаних података за цМРИ и ПЕТ (П
ЛМ11А-31 је ефикасно смањио повећање Аβ42 и Аβ40 у ЦСФ у поређењу са плацебо групом. Лек је такође показао смањење средње годишње процентуалне промене пресинаптичког протеинског биомаркера СНАП25 и смањење постсинаптичког биомаркера НГ, што указује на успоравање губитка пресинаптичких и постсинаптичких веза. ЛМ11А-31 је такође смањио раст ИКЛ40, што је резултирало смањењем ММСЕ резултата и повећаним АДАС-Цог-13 резултатима. Лек је такође смањио губитак сиве материје у фронталном режњу и задњем паријеталном кортексу и смањио метаболизам глукозе у областима као што су енторхинални кортекс, темпорални кортекс, хипокампус, острвски кортекс и префронтални кортекс.
Закључак
Студија је закључила да је модулација п75НТР помоћу ЛМ11А-31 погодна за већа клиничка испитивања. ЛМ11А-31 је испуњавао примарни безбедносни критеријум и добро су га толерисали пацијенти са благим до тешким облицима астме. Резултати указују на потребу за даљим студијама са дужим трајањем лечења како би се проценила изводљивост употребе малих молекула за регулисање п75НТР као терапије која модификује болест у АД. Студија је открила да ЛМ11А-31 значајно утиче на неколико биомаркера, укључујући Аβ40, Аβ42, СНАП25, НГ и ИКЛ40, што указује на слабљење патолошког развоја. Будуће студије могу проценити додатне показатеље здравља глија.
