Нове публикације
Једињења деривата талидомида доводе до смрти резистентних ћелија рака
Последње прегледано: 02.07.2025

Сви иЛиве садржаји су медицински прегледани или проверени како би се осигурала што већа тачност.
Имамо стриктне смјернице за набавку и само линкамо на угледне медијске странице, академске истраживачке институције и, кад год је то могуће, медицински прегледане студије. Имајте на уму да су бројеви у заградама ([1], [2], итд.) Везе које се могу кликнути на ове студије.
Ако сматрате да је било који од наших садржаја нетачан, застарио или на неки други начин упитан, одаберите га и притисните Цтрл + Ентер.
Студија коју је спровео Гете универзитет у Франкфурту указује на могућност да се деривати талидомида потенцијално могу користити за лечење рака. Талидомид се продавао као таблета за спавање педесетих година прошлог века. Касније је постао познат по томе што изазива тешке урођене мане у раним фазама трудноће.
Такође је познато да молекул обележава протеине у ћелији за уништење. Као део актуелне студије, научници су створили деривате талидомида. Успели су да покажу да ове супстанце утичу на уништавање протеина одговорних за опстанак ћелија рака.
Можда ниједан други молекул није имао тако бурну прошлост као талидомид. Био је главни састојак лека одобреног у многим земљама педесетих година прошлог века као седатив и пилула за спавање. Али убрзо је постало јасно да труднице које узимају талидомид често рађају бебе са озбиљним деформитетима.
Међутим, последњих деценија медицина је поново полагала велике наде у њега. Студије су показале, између осталог, да инхибира раст крвних судова и стога је потенцијално погодан за одсецање тумора од њихове хранљиве средине. Затим се показао веома ефикасним и у лечењу мултиплог мијелома, малигних тумора у коштаној сржи.
„Сада знамо да се талидомид може назвати 'молекуларним лепком'“, објашњава др Синглај Ченг из Института за фармацеутску хемију на Гете универзитету у Франкфурту. „То значи да је у стању да ухвати два протеина и споји их.“
Ово је посебно занимљиво јер је један од ових протеина нека врста „машине за етикетирање“: он другом протеину придаје недвосмислену ознаку „СМЕЋЕ“.
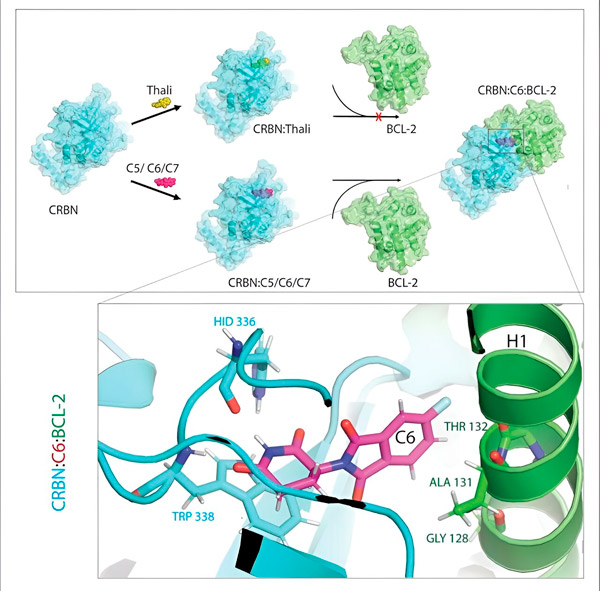
Деривати талидомида C5, C6 и C7 мењају CRBN, „машину за обележавање“, тако да се може везати за BCL-2. На овај начин, молекул BCL-2 је обележен за разградњу – могућа нова стратегија за борбу против рака. Аутор: др Синглај Ченг.
Систем за одлагање отпада ћелије препознаје ову ознаку: хвата означени протеински молекул и уситњава га. „Овај механизам објашњава различите ефекте талидомида“, каже Ченг. „У зависности од тога који је протеин означен, може изазвати деформације током ембрионалног развоја или уништити малигне ћелије.“
Овај механизам отвара велике могућности за медицину, јер ћелије рака зависе од одређених протеина да би преживеле. Ако би се могли систематски циљати и уситњавати, можда би се болест могла излечити. Проблем је што је молекуларни лепак прилично необичан.
Један од његових партнера за везивање је увек машина за обележавање ћелије, или, научним језиком, Е3 лигаза названа CRBN. Само врло мало од много хиљада протеина у телу може бити други партнер - који зависи од лепка.
„Дакле, направили смо серију деривата талидомида“, каже Ченг. „Затим смо тестирали да ли имају адхезивна својства и, ако јесу, против којих протеина су ефикасни.“ Да би то урадили, истраживачи су додали своје деривате свим протеинима у култивисаној ћелијској линији. Затим су посматрали који од ових протеина се затим разграђују у присуству CRBN-а.
„Током процеса, идентификовали смо три деривата који би могли да обележе ћелијски протеин који је веома важан за разградњу, BCL-2“, објашњава Ченг. „BCL-2 спречава ћелије да активирају свој програм самоуништења, тако да ако га нема, ћелије умиру.“
Зато је BCL-2 дуго био у фокусу истраживања рака. Постоји чак и лек за леукемију под називом венетоклакс који смањује ефикасност BCL-2 и тиме узрокује самоуништење мутираних ћелија.
„Међутим, у многим ћелијама рака, сам BCL-2 је мутиран. Као резултат тога, венетоклакс више не инхибира протеин“, каже Ченг. „Успели смо да покажемо да наши деривати такође означавају овај мутирани облик за разградњу. Поред тога, наши партнери у Институту Макс Планк за биофизику симулирали су интеракцију деривата талидомида са BCL-2 на рачунару. Ово је показало да се деривати везују за потпуно различита места од венетоклакса – резултат који смо касније могли експериментално да потврдимо.“
Истраживачи су такође тестирали своја једињења на воћним мушицама са ћелијама рака. Стопа преживљавања мушица третираних на овај начин била је знатно већа. Међутим, Ченг упозорава да се не надате превише, јер су ови резултати још увек основно истраживање. „Иако показују да модификовани молекули талидомида имају велики терапеутски потенцијал, још увек не можемо рећи да ли ће се они у неком тренутку доказати у пракси.“
Резултати студије објављени су у часопису Cell Reports Physical Science.
