Нове публикације
Разјашњење ћелијских механизама пародонтитиса помоћу побољшаног животињског модела
Последње прегледано: 02.07.2025

Сви иЛиве садржаји су медицински прегледани или проверени како би се осигурала што већа тачност.
Имамо стриктне смјернице за набавку и само линкамо на угледне медијске странице, академске истраживачке институције и, кад год је то могуће, медицински прегледане студије. Имајте на уму да су бројеви у заградама ([1], [2], итд.) Везе које се могу кликнути на ове студије.
Ако сматрате да је било који од наших садржаја нетачан, застарио или на неки други начин упитан, одаберите га и притисните Цтрл + Ентер.
Истраживачи са Токијског медицинског и стоматолошког универзитета (TMDU) развили су технику која омогућава детаљну анализу развоја пародонтитиса током времена.
Пародонтална болест, позната као пародонтитис, водећи је узрок губитка зуба и погађа скоро једну од пет одраслих особа широм света. У већини случајева, стање је резултат инфламаторног одговора на бактеријску инфекцију ткива око зуба.
Како се стање погоршава, десни почињу да се повлаче, откривајући корене зуба и кости. Приметно је да се учесталост пародонтитиса повећава са годинама, а како светска популација живи дуже, важно је имати добро разумевање његових основних узрока и прогресије.
У студији објављеној у часопису Nature Communications, истраживачи са TMDU-а пронашли су начин да постигну овај циљ побољшањем широко коришћеног животињског модела за проучавање пародонтитиса.
Директно проучавање пародонтитиса код људи је тешко. Због тога се научници често окрећу животињским моделима за претклиничке студије. На пример, „модел пародонтитиса изазваног лигатурама код миша“ омогућио је истраживачима да проучавају ћелијске механизме који леже у основи овог стања од његовог увођења 2012. године.
Једноставно речено, овај модел вештачки индукује пародонтопатију постављањем свилених нити на кутњаке мишева, што узрокује накупљање плака. Иако је ова метода погодна и ефикасна, она не обухвата потпуну слику пародонтитиса.
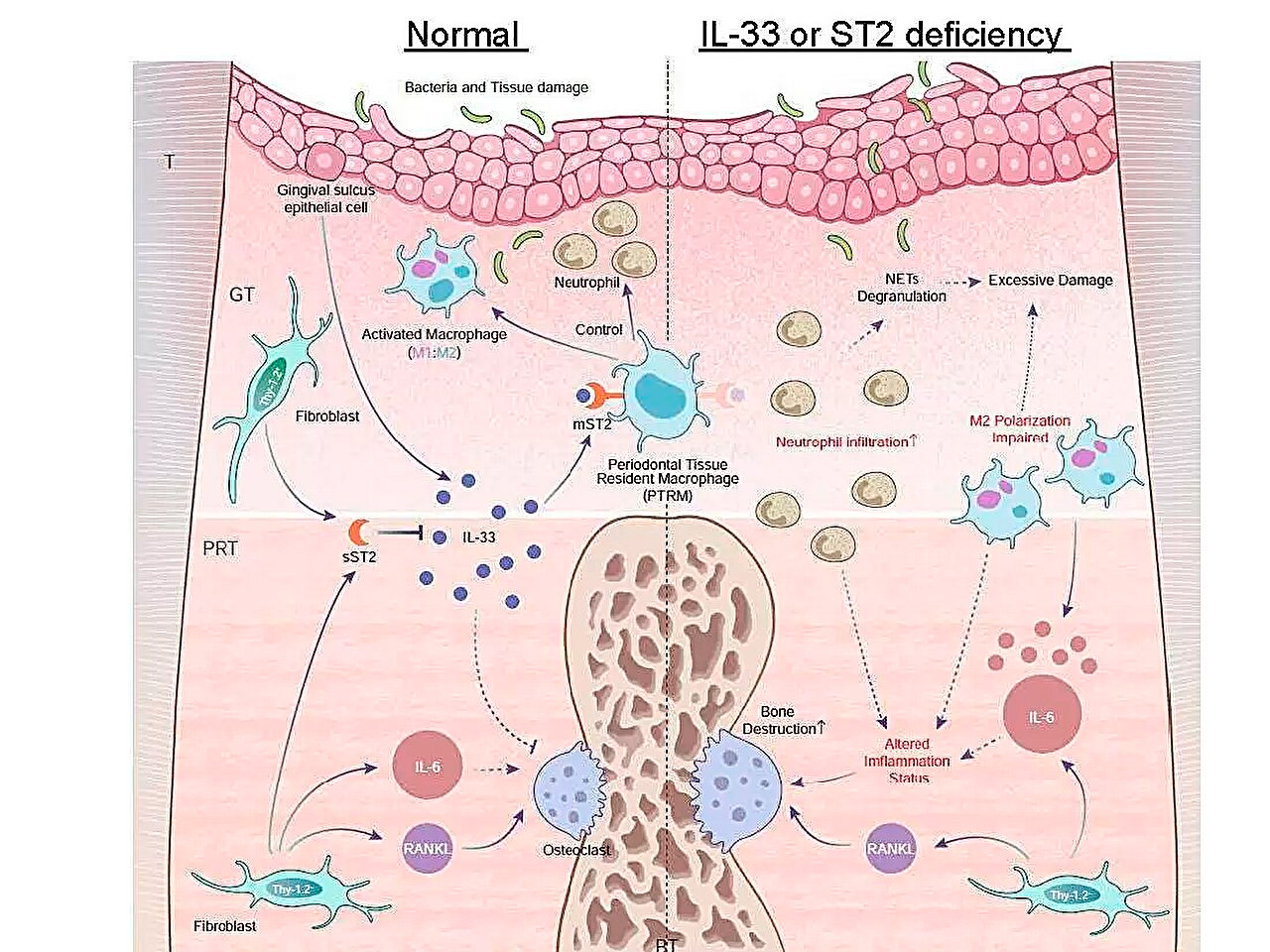
Шематски приказ профила експресије инфламаторних гена током пародонтитиса и улога IL-33/ST2 осе у борби против акутне упале. Извор: Токијски медицински и стоматолошки универзитет.
„Иако се пародонтално ткиво састоји од гингиве, пародонталног лигамента, алвеоларне кости и цемента, анализа се обично врши искључиво на узорцима гингиве због техничких и квантитативних ограничења“, напомиње водећи аутор студије Анхао Лиу. „Ова стратегија узорковања ограничава закључке који се могу извући из ових студија, тако да су потребне методе које омогућавају истовремену анализу свих компоненти ткива.“
Да би се решило ово ограничење, истраживачки тим је развио модификовани модел пародонтитиса изазваног лигатурама. Уместо класичне једне лигатуре, користили су троструку лигатуру на горњем левом кутњаку мужјака мишева. Ова стратегија је проширила подручје губитка кости без значајног уништавања кости око другог кутњака, повећавајући број различитих врста пародонталног ткива.
„Изоловали смо три главна типа ткива и проценили принос РНК између два модела. Резултати су показали да је троструко лигирани модел ефикасно повећао принос, постижући четири пута већу количину нормалног перирадикуларног ткива и подржавајући анализу високе резолуције различитих типова ткива“, објашњава виши аутор др Микихито Хајаши.
Након што су потврдили ефикасност свог модификованог модела, истраживачи су кренули да проучавају ефекте пародонтитиса на експресију гена у различитим типовима ткива током времена, фокусирајући се на гене повезане са упалом и диференцијацијом остеокласта.
Једно од њихових кључних открића било је да је експресија гена Il1rl1 била значајно већа у перирадикуларном ткиву пет дана након лигације. Овај ген кодира ST2 протеин у рецепторским и мамним изоформама, који се везује за цитокин назван IL-33, који је укључен у инфламаторне и имунорегулаторне процесе.
Да би стекли дубљи увид у улогу овог гена, тим је индуковао пародонтитис код генетски модификованих мишева којима су недостајали гени Il1rl1 или Il33. Ови мишеви су показали убрзано инфламаторно разарање костију, што истиче заштитну улогу IL-33/ST2 пута. Даља анализа ћелија које садрже ST2 протеин у његовом рецепторском облику, mST2, открила је да већина њих потиче од макрофага.
„Макрофаги се генерално класификују у два главна типа, проинфламаторне и антиинфламаторне, у зависности од њихове активације. Открили смо да су ћелије које експресују mST2 јединствене по томе што истовремено експресују неке маркере оба типа макрофага“, прокоментарисао је виши аутор др Таканори Ивата. „Ове ћелије су биле присутне у перирадикуларном ткиву пре него што је почела упала, па смо их назвали 'макрофаги који живе у пародонталном ткиву'.“
Заједно, резултати ове студије показују моћ модификованог животињског модела за проучавање пародонтитиса на детаљнијем нивоу, све до биомолекуларног нивоа.
„Предлажемо могућност новог молекуларног пута IL-33/ST2 који регулише упалу и уништавање костију код пародонталне болести, заједно са специфичним макрофагима у перирадикуларном ткиву који су дубоко укључени у пародонталну болест. Надамо се да ће ово довести до развоја нових стратегија лечења и метода превенције“, закључује главни аутор др Томоки Накашима.
