Нове публикације
Канцерогени тумор може сам себе уништити
Последње прегледано: 02.07.2025

Сви иЛиве садржаји су медицински прегледани или проверени како би се осигурала што већа тачност.
Имамо стриктне смјернице за набавку и само линкамо на угледне медијске странице, академске истраживачке институције и, кад год је то могуће, медицински прегледане студије. Имајте на уму да су бројеви у заградама ([1], [2], итд.) Везе које се могу кликнути на ове студије.
Ако сматрате да је било који од наших садржаја нетачан, застарио или на неки други начин упитан, одаберите га и притисните Цтрл + Ентер.
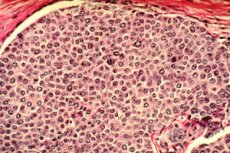
Амерички истраживачи су пронашли „слабу тачку“ у канцерогеним туморима: испоставља се да је могуће покренути програм самоуништења малигних ћелија и тиме излечити озбиљну болест.
Научници су у пацове унели ћелије људског рака дебелог црева и лимфома. Открили су да инхибиција специфичних протеинских структура које хране тумор узрокује његову смрт.
Тренутно, истраживачи већ имају готове лекове који сузбијају такву протеинску структуру као што је АТФ4. Светска медицина има све шансе да ускоро добије иновативне антитуморске агенсе који могу селективно сузбити развој малигних ћелија.
Водећи специјалиста за научни рад, др Куменис, уверио је да научници иду у правом смеру и да ће ускоро моћи потпуно да зауставе раст неоплазми без могућности рецидива тумора. Штавише, постоји поверење да је откривена „слаба тачка“ релевантна за многе онколошке патологије.
Огроман број ћелијских структура у људском телу свакодневно умире само да би заштитио друге ћелије од потенцијалних опасности. Истовремено, канцерогени тумор игнорише ово понашање имунолошке одбране. Како натерати неоплазму на самоуништење? Ово питање мучи научнике већ дуго времена. И тек сада је тим, у пратњи др Кумениса, постигао резултат повезивањем са АТФ4 у структурама црева, дојке и људског лимфома и пацова са индукованим лимфомом. Откривено је да је АТФ4 одговоран за цео биохемијски правац, функционишући истовремено са геном. Ако се овај правац заустави, малигне ћелије ће произвести велику количину протеина и умрети.
Када су научници успели да „искључе“ ATF4 у туморима и пацовима, откривено је да патолошке ћелије настављају да акумулирају протеинску супстанцу 4E-BP и потом умиру као последица стреса. Сличан механизам је „радио“ у инхибирању развоја лимфома и рака дебелог црева код животиња. Код људских тумора изазваних мутационим променама у MYC, такође је примећено повећање експресије ATF4 и 4E-BP. Др Куменис указује на улогу ове чињенице у наводном успеху открића.
Лекови који инхибирају биолошку синтезу АТФ4 (скраћеница од активирајући транскрипциони фактор 4) нису нови; производе их фармацеутске компаније и користе се за лечење многих патологија, укључујући Алцхајмерову и Паркинсоновуболест.
Према резултатима истраживања, утицај на ATF4 је ефикасан у односу на MYC-зависне неоплазме. Тренутно се спроводе експерименти како би се утврдили могући нежељени ефекти таквог лечења код пацијената оболелих од рака.
Резултати научног рада објављени су у часопису Sciencedaily.
