Медицински стручњак за чланак
Нове публикације
Глиом мозга
Последње прегледано: 29.06.2025

Сви иЛиве садржаји су медицински прегледани или проверени како би се осигурала што већа тачност.
Имамо стриктне смјернице за набавку и само линкамо на угледне медијске странице, академске истраживачке институције и, кад год је то могуће, медицински прегледане студије. Имајте на уму да су бројеви у заградама ([1], [2], итд.) Везе које се могу кликнути на ове студије.
Ако сматрате да је било који од наших садржаја нетачан, застарио или на неки други начин упитан, одаберите га и притисните Цтрл + Ентер.
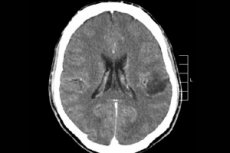
Међу многим туморским процесима централног нервног система, најчешће се дијагностикује глиом мозга - овај термин је колективни, неоплазма обједињује све дифузне олигодендроглијалне и астроцитне фокусе, астроцитом, астробластом и тако даље. Такав тумор може имати различит степен малигнитета, формиран је од глијалних структура - ћелија локализованих око неурона. Главно подручје локализације глиома су мождане хемисфере, зидови можданих комора и хијазма - подручје делимичног пресека влакана оптичког нерва. Споља, тумор је нодуларни елемент ружичасте или црвенкасте нијансе, округле или вретенасте конфигурације са нејасним границама. [ 1 ]
Епидемиологија
У око 5% случајева, глиоми су повезани са наследним патологијама - посебно, неурофиброматозом и другим синдромима са доминантним наслеђивањем. Стручњаци истичу да се апсолутна већина глиома мозга развија спорадично - то јест, без јасног узрока.
Генерално, примарне неоплазме централног нервног система чине приближно 2% свих тумора, или нешто више од 21 случаја на сто хиљада становника. Међу њима, глиоми се јављају у 35-36% случајева, а више од 15% њих су глиобластоми.
Према неким подацима, глиом чешће погађа мушкарце него жене - тумор је посебно чест код људи старијих од 50 година.
Глобална инциденца глиома међу старијим особама значајно је порасла последњих деценија. Разлози за ову појаву још увек нису утврђени.
Према дефиницији Светске здравствене организације, идентификоване су три главне варијанте глијалних тумора, које се разликују по својим хистолошким карактеристикама. То су олигодендроглиоми, астроцитоми и комбиновани олигоастроцитоми. Учесталост сваког подтипа ниске малигне патологије није поуздано утврђена. Неке студије указују на повећање учесталости олигодендроглиома од 5% до 30% и смањење учесталости астроцитома.
Глијални тумори су способни да инфилтрирају мождано ткиво, а велика већина нискостепених жаришта постаје малигна у року од неколико година. [ 2 ]
Узроци глиома мозга
Глиом мозга је читава група туморских процеса, чија је заједничка карактеристика њихово формирање из глијалних структура ЦНС-а које се налазе у можданом ткиву. Такви тумори су подељени у две хистопатолошке варијанте: високо малигни и ниско малигни глиоми.
Извор формирања раста су ћелије неуроглије (астроцити, олигодендроцити), које пружају структурну основу и одрживост можданих неурона.
Глијални туморски процеси се значајно разликују по структури, мутационим променама у генима, агресивности, клиничким карактеристикама, дијагностичким карактеристикама, одговору на лечење и прогнози пацијената. Ембрионалне и епендималне неоплазме централног нервног система - посебно медулобластоми и епендимоми - разликују се по својој хистолошкој структури, али су сличне у погледу лечења.
Глијални елементи су први пут класификовани као засебна структурна категорија нервног система крајем 19. века.
Неуроглијско ткиво се састоји од ћелија које имају помоћне функције: трофичке, потпорне, заштитне, секреторне. Неурони и глиоцити постоје заједно једни са другима, заједно чине нервни систем и имају велики значај у општим процесима виталне активности организма.
Глиоцити се грубо категоришу у неколико главних облика: астроцити, олигодендроцити, епендималне ћелије и микроглија.
До данас, научници не могу да одговоре на питање о поузданим узроцима формирања неуроглијалних тумора. Претпоставља се да одређени негативан допринос дају радиоактивни ефекти, заразне болести, интоксикације (посебно хемијска, професионална). Наследни фактор је такође важан.
Глиоми мозга настају од абнормалних неуроглиоцита који имају генетски дефект који доводи до абнормалног раста и функционалности - такве структуре се називају „незреле“. Непотпуне ћелије се чешће налазе у једном подручју, где се тумор формира.
Једноставно речено, формирање глијалних ћелија је резултат хаотичног и спорадичног раста модификованих неуроглијских ћелија. Процес се може развити из епендимоцита, олигодендроцита, астроцита (астроцитом, укључујући гигантоцелуларни и анапластични). [ 3 ]
Фактори ризика
Упркос чињеници да стручњаци не могу прецизно окарактерисати узроке настанка глијалних онкопатологија, у неким случајевима њихова појава се може спречити елиминисањем главних фактора ризика:
- Излагање јонизујућем зрачењу има канцерогено дејство, може изазвати развој леукемије и формирање канцерогених процеса са густом структуром, укључујући и код особа младог узраста. Честе и неразумне радиолошке медицинске процедуре, ултраљубичасто зрачење (укључујући соларијум) такође спадају у потенцијалне канцерогене ефекте и могу изазвати појаву тумора у различитим органима, укључујући и мозак.
- Професионални штетни ефекти, интоксикације често имају узрочну везу са развојем канцерогених тумора. Производња гуме и стакла, пестицида и горива, метала и текстила, боја и лабораторијских реагенса сматра се посебно опасном. У ризику су радници у ваздухопловној, угљеној и металској индустрији, постројењима за производњу хемијских производа и нуспроизвода, грађевинских материјала и електрода, горива и мазива, пластике и мономера.
- Загађење ваздуха, воде и земљишта одговорно је за чак 4% свих канцерогених патологија у свету. Канцерогени, присутни у великим количинама у животној средини, улазе у организам удисаним ваздухом, водом за пиће и храном. Живот у еколошки небезбедним подручјима - у близини великих индустријских објеката, прометних транспортних чворишта - сматра се посебно опасним.
- Инфективне патологије - посебно вирусне инфекције - такође могу створити услове погодне за развој тумора. Важно је имати ово на уму и вакцинисати се унапред, као и спречити заразне и паразитске болести.
- Дуван и алкохолна интоксикација се сматрају факторима ризика за многе врсте рака, не само за глиоме мозга.
- Недовољна физичка активност, прекомерна тежина, неправилна исхрана, метаболички поремећаји, повреде главе, васкуларне патологије - додатни фактори стреса који могу изазвати почетак интрацелуларних поремећаја.
- Старије доба је најчешћи период за развој неоплазми у телу, тако да би они старији од 55 година требало посебно да воде рачуна о сопственом здрављу.
Међутим, главни и најзначајнији фактор ризика за развој глиома остаје наследна предиспозиција.
Патогенеза
До данас, стручњаци имају низ претпоставки у вези са развојем глиома мозга. Свака теорија има своје основне основе, али једини исправан и поуздан патогенетски механизам научници још увек нису идентификовали. У већини случајева, говоримо о следећим факторима у развоју неоплазми:
Неуспех ембриогенезе, који се састоји у поремећају полагања органа и формирању „погрешних“ ћелијских структура;
- Изложеност јонизујућем зраку, потенцијалним канцерогенима у облику хемијских агенаса, адитива за храну итд.;
- Траума главе;
- Генски поремећаји који се преносе са генерације на генерацију („фамилијарни“ глиом);
- Имунолошка дисфункција, неуроинфекције.
Већина глиома има дифузни раст, са пенетрацијом у околно нормално мождано ткиво. У зависности од степена малигнитета, тумор се може развијати неколико година без икаквих манифестација. У случају агресивног тока, симптоматологија се брзо повећава током неколико месеци.
Део туморогенезе је последица дисембриогенетских промена.
Мождано стабло може бити захваћено на различитим нивоима: дифузни глиом можданог стабла, заузврат, разликоваће се и анатомо-морфолошки и клинички. Неке такве неоплазме - посебно глиом квадриплегијске плоче - могу бити релативно бенигне, без знакова прогресије. С друге стране, понтински глиом карактерише се посебном малигнитетом, агресивношћу и лошом прогнозом.
Дифузне лезије можданих структура, у којима је више од три анатомске зоне великих хемисфера укључено у патолошки процес, са могућом перивентрикуларном дивергенцијом и проласком кроз корпус мозга, називају се глиоматоза. [ 4 ]
Да ли је глиом мозга наследан?
Добро доказан ризик од формирања глиома мозга је наследан - то јест, присуство сличних или других интрацеребралних тумора код директних предака или у истој генерацији. Радиоактивна изложеност и редован или продужени контакт са потенцијалним канцерогенима погоршавају ситуацију.
Не само да се глиоми могу наследити, већ и болести које су праћене повећаним растом тумора без позивања на локализацију - посебно, ово може бити неурофиброматоза типа 1 и 2, Ли-Фраумени синдром, Хипел-Линдау. Често се у ћелијама глиома откривају промене у одређеним генима или хромозомима.
Главне патологије које су повезане са развојем глиома код људи сумиране су у табели:
Патологија |
Хромозом |
Џин |
Разноврсност неоплазми |
Ли-Фраумени синдром |
17р13 |
TR53 |
Неуроектодермалне неоплазме, астроцитом. |
Неурофиброматоза |
17q11 |
НФ1 |
Глиом оптичког нерва, пилоцитни астроцитом, неурофиброматоза |
Туркотов синдром |
3p21, 7p22 |
ХМЛХ1, ХПСМ2 |
Астроцитом |
Туберозна склероза (Бурневилов синдром). |
9q34, 16p13 |
ТСЦ1, ТСЦ2 |
Гигантоцелуларни субепендимални астроцитом |
Без обзира на природу глијалног тумора, да ли је у питању спорадични случај или наследна патологија, реч је о поремећају са експресијом патолошки измењеног гена. Осим неоплазми насталих као резултат ефеката учења, у другим ситуацијама узроци генетских промена остају нејасни.
Симптоми глиома мозга
Карактеристике фокалне симптоматологије директно зависе од подручја локализације глиома мозга и постају последица свих врста ендокриних поремећаја, компресије нервног ткива или локалних деструктивних процеса.
Ако се неоплазма налази у паријеталној зони, онда код особе доминирају манифестације као што су напади, сензорни поремећаји, оштећење слуха.
Када је глиом локализован у подручју доминантне хемисфере, откривају се поремећаји говора, аграфија, агнозија.
Неоплазме темпоралног режња често су праћене конвулзивним нападима, афазијом, оштећеним чулом мириса и визуелном функцијом и диспнејом.
Када се интракранијални притисак повећа, развија се одговарајућа слика са ограничењем видних поља, парализом очних мишића и хемиплегијом.
Због специфичности туморског процеса, глиом мозга је увек праћен неуролошким симптомима у већој или мањој мери. У почетку је приметна општа слабост, пацијент стално жели да спава, способност за рад је оштећена, мисаони процеси су успорени. Управо у овој фази постоји висок ризик од постављања погрешне дијагнозе и, као последица тога, прописивања погрешног лечења. Међу осталим неспецифичним манифестацијама:
- Вестибуларни поремећаји, укључујући нестабилан ход, губитак равнотеже (нпр. приликом вожње бицикла или пењања степеницама), утрнулост у удовима итд.;
- Постепено погоршање вида, удвостручавање визуелне слике;
- Погоршање слушне функције;
- Нејасан говор;
- Мучнина и повраћање у облику напада независно од хране или пића;
- Слабљење мимичких мишића и других мишића лица;
- Нелагодност приликом гутања;
- Редовне главобоље (често у јутарњим сатима).
Клиничка слика се постепено шири и погоршава: код неких пацијената се то дешава споро, код других - нагло, буквално „пред њиховим очима“, у року од неколико недеља. У овом другом случају говоримо о агресивном, брзо развијајућем глиому мозга.
Први знаци
Глиом мозга у раним фазама развоја нема изражену симптоматологију. Прве манифестације се често погрешно тумаче за знаке других, мање опасних патологија.
Генерално, клиничка слика глиома је разнолика и одређена је локацијом и величином патолошког жаришта. Како неоплазма расте, развијају се и повећавају се општи церебрални симптоми:
- Упорни и редовни бол у глави који не реагује на стандардне лекове (нестероидни антиинфламаторни лекови);
- Повремена мучнина, понекад до тачке повраћања;
- Непријатан, тежак осећај у пределу очне јабучице;
- Напади.
Церебралне манифестације су посебно интензивне када тумор расте у коморе или ликворни систем. Дренажа цереброспиналне течности је оштећена, интракранијални притисак се повећава, развија се хидроцефалус. Процес погађа одређени део мозга, што утиче на развој одговарајуће клинике:
- Постоје проблеми са визуелном функцијом;
- Оштећен говор;
- Јављају се вестибуларни поремећаји (вртоглавица, поремећена координација покрета);
- Пареза, парализа руку, ногу;
- Памћење и концентрација су оштећени;
- Мисаони процеси су поремећени;
- Појављују се поремећаји понашања.
У почетној фази, симптоми су практично одсутни, или су толико безначајни да не привлаче пажњу. Управо због тога стручњаци снажно саветују редовне превентивне прегледе и контроле. На крају крајева, што се раније открије туморски процес, веће су шансе за излечење и преживљавање. [ 5 ]
Глиом мозга код детета
Међу многим туморима мозга који се налазе у детињству, проценат глиома се креће од 15 до 25%. Деца могу добити болест у раним тинејџерским и раним двадесетим годинама, мада је веома ретко да бебе млађе од 3 године оболе од болести.
Патологија почиње на позадини мутације глијалних ћелија. До данас нема одговора на питање зашто се ова мутација јавља.
Једино што је поуздано научено јесте да одређене наследне болести повезане са повећаним ризиком од раста тумора повећавају и вероватноћу развоја глиома мозга.
Поред тога, научници су открили да глијалне ћелије могу имати дивергенцију у појединачним генима или хромозомима. Због овог поремећаја, активира се механизам мутације, који није наследан. Могуће је да се то дешава у једној од најранијих фаза развоја.
Доказана је чињеница да присуство акутне леукемије или ретинобластома у историји детета, или зрачење мозга из било ког другог разлога, значајно повећава ризике од формирања глиома (након одређеног временског периода).
Симптоматологија у детињству зависи од степена малигнитета и локализације патолошког жаришта. Разликују се специфични и неспецифични симптоми:
- Неспецифични симптоми нису „везани“ за подручје где се налази глиом. Уобичајене манифестације могу укључивати главобољу, вртоглавицу, слаб апетит, повраћање без везе са уносом хране, губитак тежине (из непознатих разлога), стални осећај умора, пад академског успеха, тешкоће у концентрацији, поремећаје у понашању. Ови знаци су последица компресије интракранијалних структура, што се може објаснити као директан притисак растуће масе, и поремећај у циркулацији цереброспиналне течности. Постоји ризик од церебралне хидроцеле.
- Специфична симптоматологија зависи од непосредне локације глијалног патолошког жаришта. На пример, тумор малог мозга је обично праћен оштећеним ходом и равнотежом код деце. Лезија великог мозга се манифестује конвулзивним нападима, а раст тумора у кичменој мождини - парализом мускулатуре. Дешава се да се беби нагло погорша вид, поремети свест, поремети сан или се појави неки други проблем у развоју.
По правилу, у детињству, малигни глиом се открива за неколико недеља или месеци свог развоја: често се карактерише брзим и неконтролисаним растом неоплазме.
Децу са малигним глијалним туморима лече лекари у педијатријским клиничким центрима специјализованим за педијатријску онкологију. По правилу се користе хируршко лечење, радиотерапија и курсеви хемотерапије.
Најважнији корак у лечењу је неурохирургија. Што је радикалнија, веће су шансе детета за излечење. Али хируршка интервенција није увек могућа: посебно се могу јавити проблеми са уклањањем глиома можданог стабла, као и са зрачењем код деце млађе од 3 године.
Глиоме централног мозга (средњег и средњег мозга) је тешко потпуно уклонити, јер постоји ризик од оштећења здравог ткива. Ако је потпуна ресекција тумора немогућа, пацијенту се прописује палијативни третман.
Деца са малигним глиомима лече се према стандардизованим протоколима који су утврђени кроз ригорозно контролисана клиничка испитивања. Најчешћи протоколи су следећи:
- ХИТ ХГГ 2007: обухвата лечење деце узраста од 3 до 17 година.
- ХИТ СКК: погодно за одојчад (до три године) и не укључује радиотерапију.
Статистика преживљавања деце код глиома генерално није баш оптимистична. Међутим, ни у ком случају није могуће унапред предвидети ефикасност мера лечења за одређено дете. Важно је пажљиво пратити сва лекарска упутства, што значајно повећава шансе за опоравак.
Обрасци
Глиоми могу бити ниско малигни и високо малигни, са интензивним растом и склоношћу ка метастазирању. Важно је разумети да низак малигнитет није синоним за безбедност тумора. Свака неоплазма мозга ствара додатни волумен, стиска мождане структуре, што доводи до њиховог померања и повећаног интракранијалног притиска. Као резултат тога, пацијент може умрети.
Постоје два главна типа малигних астроцитома. То су глиобластоми и анапластични астроцитоми, који се деле према молекуларним променама. Секундарни малигни тумори који су се развили из астроцитома и имају низак степен малигнитета најчешће се налазе код младих пацијената. Иницијално малигни тумори глијалног типа чешће се јављају код старијих пацијената.
У зависности од структурне локације, глиоми се деле на:
- Супратенторијални (са локализацијом изнад малог мозга у пределу латералних комора, великих хемисфера);
- Субтенторијални (са локализацијом испод малог мозга у задњој кранијалној јами).
Према хистолошким карактеристикама, разликују се следеће врсте глиома:
- Астроцитни глиом је најчешћи. Заузврат, подељен је на нодуларни и дифузни (последњи се може окарактерисати брзим растом и обрасцем можданог удара).
- Олигодендроглиом - јавља се код 5% пацијената. Има петрификате - подручја калцификације, најчешће у фронталном режњу.
- Епендимални глиом - расте из структура које облажу зидове централног канала кичмене мождине и комора. Често расте у дебљину мождане супстанце, као и у лумен мозга.
Такође су могућа мешана патолошка жаришта као што су субепендимом, олигоастроцитом итд.
Сви глиоми су категорисани у следеће фазе:
- Споро растуће релативно бенигне неоплазме без очигледних клиничких симптома.
- Споро растући „гранични“ глиоми који се постепено трансформишу у трећи стадијум и даље.
- Малигни глиом.
- Малигни глиом са интензивним агресивним растом и ширењем, са лошом прогнозом.
Што је стадијум малигнитета нижи, мања је вероватноћа метастаза и рецидива уклоњене неоплазме, а веће су шансе за излечење пацијента. Највећу опасност представља мултиформни глиобластом, ниско диференцирани процес са интензивним растом и развојем. [ 6 ]
Могуће и најчешће варијанте неуроглиома:
- Глиом са лезијама можданог стабла и моста налази се у подручју где се мозак спаја са кичменом мождином. Управо тамо су локализовани важни неуроцентри одговорни за респираторне, срчане и моторичке функције. Ако је ова зона оштећена, поремећен је рад вестибуларног и говорног апарата. Често се открива у детињству.
- Визуелни глиом утиче на неуроглијалне ћелије које окружују оптички нерв. Патологија узрокује оштећење вида и егзофталмос. Чешће се развија код деце.
- Ниски малигни неуроглиом карактерише спори раст, локализован је чешће у великим хемисферама и малом мозгу. Чешће се јавља код младих особа (адолесценти и млади одрасли око 20 година).
- Глиом corpus callosum-а је карактеристичнији за особе између 40 и 60 година и најчешће је представљен глиобластомом.
- Глиом хијазме је локализован у зони оптичког споја, па је праћен миопијом, губитком видног поља, оклузивним хидроцефалусом и неуроендокриним поремећајима. Може се јавити у било ком узрасту, али најчешће погађа пацијенте са неурофиброматозом типа I.
Компликације и посљедице
Глиоми ниског малигнитета (степен I-II, високо малигни - нпр. астроцитом, олигоастроцитом, олигодендроглиом, плеоморфни ксантоастроцитом, итд.) и високог малигнитета (степен III-IV - глиобластом, анапластични олигодендроглиом, олигоастроцитом и астроцитом). Глиоми IV степена су посебно малигни.
Глиом можданог стабла има веома неповољну прогнозу управо зато што неоплазма погађа такав регион мозга, где су концентрисане најважније нервне везе између мозга и удова. Чак је и прилично мали тумор у овој области довољан да брзо погорша стање пацијента и изазове парализу.
Ништа мање неповољне последице се јављају када су захваћени и други региони мозга. Често је у питању тумор мождане коре, који не даје шансе за дуг животни век пацијента, упркос лечењу. Често је могуће само одложити смрт.
Према медицинској статистици, петогодишња стопа преживљавања је често само 10-20%. Иако ове бројке у великој мери зависе и од степена малигнитета и од тачне локализације и обима извршене хируршке интервенције. Након потпуног уклањања патолошког фокуса, стопа преживљавања значајно се повећава (понекад - и до 50%). Недостатак лечења или његова немогућност (из једног или другог разлога) гарантовано доводи до смрти пацијента.
Већина нискомалигних глијалних тумора може да инфилтрира мождано ткиво и малигнизује се током неколико година.
Стручњаци сматрају да је ризик од поновног појављивања глиома „врло вероватан“. Ипак, лечење не треба занемарити: важно је обезбедити добар квалитет живота што је дуже могуће.
Рекурентни глиоми увек имају лошију прогнозу од примарних тумора. Међутим, савремени протоколи лечења засновани на студијама терапијске оптимизације често постижу довољно добре резултате код пацијената чак и са високо малигним неоплазмама.
Могући исходи након хемотерапије:
- Мршавост, изгладнелост, поремећаји варења, болести усне дупље;
- Повећана ексцитабилност централног нервног система, астенија;
- Погоршање функције слуха, тинитус и зујање у ушима;
- Напади, депресивни поремећаји;
- Хипертензивна криза, промена у крвној анализи;
- Бубрежна инсуфицијенција;
- Алергијски процеси, губитак косе, појава пигментних мрља на телу.
Након хемотерапије, пацијенти примећују изражено слабљење имуног система, што може изазвати развој разних заразних патологија.
Дијагностика глиома мозга
Глиом мозга може се посумњати на основу следећих знакова:
- Пацијент има локализоване или генерализоване нападе, који су карактеристични за кортикалну локацију неоплазме и њен спори развој. Епи-напади се налазе код 80% пацијената са глијалним туморима ниског степена и код 30% пацијената са глиомима високог степена.
- Повишен интракранијални притисак је посебно карактеристичан за масе које се налазе у десном фронталном и паријеталном режњу. Поремећај циркулације крви и циркулације ликвора, повезан са високим интракранијалним притиском, подразумева појаву сталног и све већег бола у глави, мучнине са повраћањем, поремећаја вида, поспаности. Јавља се едем очног нерва, парализа одводног нерва. Повећање интракранијалног притиска на критичне вредности може довести до развоја коме и смрти. Још један узрок високог интракранијалног притиска је хидроцефалус.
- Пацијент има растућу фокалну слику. У супратенторијалним формацијама, поремећене су моторне и сензорне сфере, хемиопија, афазија, когнитивни поремећаји напредују.
Ако лекар посумња на присуство неоплазме мозга, оптимално је извршити МРИ без или са увођењем контрастног средства (гадолинијума) како би се сазнала његова локација, величина и додатне карактеристике. Ако снимање магнетном резонанцом није могуће, врши се компјутерска томографија, а као метода диференцијације користи се магнетна резонантна спектроскопија. Упркос информативности ових дијагностичких метода, коначна дијагноза се поставља тек након хистолошке потврде током ресекције фокуса тумора.
С обзиром на горе наведене критеријуме, препоручује се да се дијагноза започне темељном анамнезом, проценом сомато-неуролошког статуса и функционалног статуса. Неуролошки статус се процењује уз утврђивање вероватних интелектуалних и мнестичких поремећаја.
Препоручени лабораторијски тестови:
- Комплетна општа клиничка анализа крви;
- Комплетан биохемијски тест крви;
- Анализа урина;
- Студија коагулације крви;
- Анализа онколошких маркера (АФП, бета-хЦГ, ЛДХ - релевантно ако се сумња на лезију пинеалне зоне).
Да би се разјасниле прогностичке тачке код пацијената са глиобластомом и анапластичним астроцитомом, процењују се мутација гена IDH1|2-1 и метилација гена MGMT. Код пацијената са олигодендроглиомом и олигоастроцитомом, одређује се коделација 1p|19q.
Инструментална дијагностика, пре свега, представљена је обавезним снимањем магнетне резонанце мозга (понекад - и кичмене мождине). МРИ се изводи у три пројекције користећи стандардне Т1-2, ФЛАИР, Т1 режиме са контрастом.
Када је индиковано, изводе се ултразвук васкуларне мреже, функционална магнетна резонанца моторног и говорног дела, као и ангиографија, спектроскопија, МР трактографија и перфузија.
Додатна истраживања могу укључивати:
- Електроенцефалографија мозга;
- Консултације са неурохирургом, онкологом, радиологом, офталмологом, радиологом.
Диференцијална дијагноза
Диференцијална дијагноза се нужно спроводи са нетуморским патологијама - посебно са крварењем узрокованим артерио-венском или артеријском малформацијом, као и са псеудотуморским демијелинизирајућим процесима, инфламаторним болестима (токсоплазмоза, апсцес мозга итд.).
Поред тога, разликујте примарни фокус тумора и метастазе централног нервног система.
Са савременим могућностима магнетне резонанце, могуће је довољно прецизно извршити дијагностичке мере, открити порекло примарног фокуса у ЦНС-у. МРИ мозга се изводи са или без контраста, у Т1, Т2 ФЛАИР режиму - у три пројекције, или танким кришкама у аксијалној пројекцији (СПГР режим). Ове дијагностичке методе омогућавају прецизно одређивање локације, величине, структурних карактеристика неоплазме, њеног односа са васкуларном мрежом и оближњим областима мозга.
Поред тога, ЦТ (са или без контраста), ЦТ ангиографија (МР ангиографија), МР трактографија, МР или ЦТ перфузија могу се извршити као део диференцијалне дијагнозе. ЦТ/ПЕТ мозга са метионином, холином, тирозином и другим аминокиселинама се користи када је индиковано.
Третман глиома мозга
Специфична терапија се састоји од хируршких, хемотерапеутских и зрачних мера. Обавезно је, ако је могуће, извршити потпуну ресекцију туморског жаришта, што омогућава брзо ублажавање симптома и хистолошку потврду дијагнозе.
Зрачење позитивно утиче на повећање животног века пацијената. Стандардно се примењује укупна доза од 58 до 60 Gy, подељена на појединачне дозе зрачења од 1,8-2 Gy. Тумор се зрачи локално, додатно захватајући до 3 цм око њега. Радиотерапија је прихватљивија за разлику од брахитерапије. У неким случајевима се препоручују радиохируршке методе, које се састоје од зрачења гама ножем или линеарним гас педалом, као и терапије бором са неутронским захватом.
Потреба за адјувантном хемотерапијом је контроверзна. У неким случајевима, препарати нитрозоуреје су омогућили повећање животног века пацијената до годину и по дана, али су неки резултати коришћења таквих хемопрепарата били негативни. Данас се активно користе цитотоксични агенси, неоадјувантна терапија (пре зрачења), комбиновани лекови, интраартеријска хемотерапија или хемотерапија високих доза са даљом трансплантацијом матичних ћелија.
Генерално, за успешно лечење глиома, веома је важан свеобухватан приступ, чији обим зависи од локације и степена малигнитета масе, њене величине и општег здравственог стања пацијента.
У вези са глиомом можданог стабла, хируршка интервенција се ретко користи. Главна контраиндикација за операцију је подручје локализације жаришта - у непосредној близини виталних делова. У неким случајевима могуће је уклонити глиом трупа микрохируршким методама, уз преоперативну и постоперативну хемотерапију. Таква интервенција је веома сложена и захтева посебне квалификације неурохирурга.
Радиохирургија, а посебно стереотактичка хирургија са излагањем високим јонизујућим дозама, је прилично ефикасна. Употреба такве технике у раним фазама развоја неоплазме понекад омогућава постизање продужене ремисије или чак потпуног излечења пацијента.
Зрачење се често комбинује са хемотерапијом, што побољшава ефикасност интервенција и смањује оптерећење зрачењем. Код глиома, нису сва хемопревентивна средства терапеутски успешна, па се прописују појединачно, а рецепти се прилагођавају ако је потребно.
Да би се смањио бол и смањио интракранијални притисак, без обзира на главни третман, прописује се симптоматска терапија - посебно кортикостероидни лекови, аналгетици, седативи.
Лекови
Кортикостероидни лекови утичу на оток, смањују тежину неуролошких симптома током неколико дана. Међутим, због вишеструких нежељених ефеката и повећане вероватноће нежељених интеракција са хемотерапијским лековима, користе се минимално ефикасне дозе стероида, а њихова примена се прекида што је пре могуће (нпр. након операције).
Антиконвулзиви се систематски користе као секундарна превентивна мера код пацијената који су већ доживели епилептичке нападе. Ови лекови могу изазвати озбиљне нежељене симптоме и такође могу да интерагују са лековима за хемотерапију.
Антикоагуланси су посебно релевантни у постоперативној фази, јер су ризици од формирања тромбофлебитиса код глиома прилично високи (до 25%).
Добар ефекат се очекује од узимања антидепресива-анксиолитика. Употреба метилфенидата 10-30 мг/дан у две дозе често омогућава оптимизацију когнитивних способности, побољшање квалитета живота, одржавање радног капацитета.
Неуролошки поремећај и знаци церебралног едема (бол у глави, поремећаји свести) елиминишу се кортикостероидним лековима - посебно преднизолоном или дексаметазоном. |
Шема и дозирање кортикостероида се бирају индивидуално, уз праксу минималне ефикасне дозе. На крају курса лечења, лекови се постепено укидају. |
Кортикостероиди се узимају заједно са гастропротективним лековима - блокаторима протонске пумпе или блокаторима Х2-хистамина. |
Диуретици (Фуросемид, Манитол) се прописују за јак оток и померање можданих структура, као додатак кортикостероидним лековима. |
У случају конвулзивних напада (укључујући анамнезу) или епилептиформних симптома на електроенцефалограму, додатно се прописује антиконвулзивна терапија. Антиконвулзиви се не прописују у профилактичке сврхе. |
Пацијентима са индикацијама за хемотерапију препоручује се узимање антиконвулзива који не утичу на функцију ензима јетре. Лекови избора: Ламотригин, Валпроинска киселина, Леветирацетам. Не треба користити: Карбамазепин, Фенобарбитал. |
Главобоља код глиома мозга се лечи кортикостероидима. |
У неким случајевима главобоље могу се користити нестероидни антиинфламаторни лекови или трамадол. |
Ако пацијент узима нестероидне антиинфламаторне лекове, они се прекидају неколико дана пре операције како би се смањила могућност крварења током операције. |
У одабраним случајевима бола, могу се препоручити наркотични аналгетици - као што су фентанил или тримеперидин. |
Да би се спречила плућна емболија од трећег дана након операције, прописује се примена хепарина мале молекулске тежине - посебно, натријума еноксапарина или калцијума надропарина. |
Ако је пацијент на систематској антикоагулантној или антиагрегантној терапији, прелази на хепарине мале молекулске тежине најкасније недељу дана пре хируршке интервенције, са њиховим даљим повлачењем дан пре операције и наставком 24-48 сати након операције. |
Ако пацијент са глиомом има венску тромбозу доњих екстремитета, спроводи се лечење директним антикоагулансима. Није искључена могућност постављања CAVA-филтера. |
Хемотерапија за малигне глиоме мозга
Основни антитуморски хемотерапијски режими за глиоме сматрају се следећим:
- Ломустин 100 мг/м² првог дана, винкристин 1,5 мг/м² првог и осмог дана, прокарбазин 70 мг/м² од осмог до двадесет првог дана, циклуси сваких шест недеља.
- Ломустин 110 мг/м² сваких шест недеља.
- Темозоломид 5/23 150 до 200 мг/м² од првог до петог дана, сваких 28 дана.
- Темозоломид као део хеморадиотерапије, 75 мг/м² сваког дана када се примењује зрачење.
- Темозоломид са цисплатином или карбоплатином (80 мг/м²) и темозоломид 150-200 мг/м² од 1. до 5. дана сваке 4 недеље.
- Темозоломид 7/7 у дози од 100 мг/м² од 1. до 8. и од 15. до 22. дана курса, са понављањем сваке четири недеље.
- Бевацизумаб 5 до 10 мг/кг првог и петнаестог дана, и иринотекан 200 мг/м² првог и петнаестог дана, понављано сваке четири недеље.
- Бевацизумаб 5 до 10 мг/кг првог, петнаестог и двадесет деветог дана, и Ломустин 90 мг/м² првог дана сваких шест недеља.
- Бевацизумаб 5 до 10 мг/кг првог и петнаестог дана, Ломустин 40 мг првог, осмог, петнаестог и двадесет другог дана, понављано сваких шест недеља.
- Бевацизумаб 5 до 10 мг/кг првог и петнаестог дана, понављати сваке четири недеље.
Цитостатски лекови у многим случајевима успешно инхибирају раст туморских ћелија, али не показују селективност према здравим ткивима и органима. Стога су стручњаци идентификовали низ контраиндикација код којих је хемотерапија глиома немогућа:
- Прекомерна индивидуална осетљивост на хемопревентивне агенсе;
- Декомпензација срчане, бубрежне, јетрене функције;
- Депресивна хематопоеза у коштаној сржи;
- Проблеми са функцијом надбубрежне жлезде.
Хемотерапија се примењује са изузетним опрезом:
- Пацијенти са значајним поремећајима срчаног ритма;
- Са дијабетесом;
- За акутне вирусне инфекције;
- Код старијих пацијената;
- Пацијенти који пате од хроничног алкохолизма (хронична алкохолна интоксикација).
Најозбиљнији нежељени ефекат хемопревентивних лекова је њихова токсичност: цитостатици селективно ометају функционалност крвних зрнаца и мењају њихов састав. Као последица тога, маса тромбоцита и еритроцита се смањује и развија се анемија.
Пре него што пацијенту пропише курс хемотерапије, лекар увек узима у обзир степен токсичности лекова и вероватне компликације након њихове употребе. Курсеви хемотерапије увек се пажљиво прате од стране специјалиста и редовно се прати крвна слика.
Могуће последице цитостатске терапије:
- Мршавост, изгладнелост;
- Тешкоће са гутањем хране, суве слузокоже, пародонтитис, диспепсија;
- Нестабилност централног нервног система, манично-депресивни поремећаји, синдром нападаја, астенија;
- Погоршање слушне функције;
- Повећање крвног притиска до развоја хипертензивне кризе;
- Смањење броја тромбоцита, црвених крвних зрнаца, белих крвних зрнаца, вишеструка крварења, унутрашње и спољашње крварење;
- Бубрежна инсуфицијенција;
- Алергијски процеси;
- Губитак косе, појава подручја повећане пигментације.
Након курсева хемотерапије, пацијенти имају повећан ризик од развоја заразних болести, а болови у мишићима и зглобовима су чести.
Да би се смањио ризик од нежељених постхемотерапеутских ефеката, нужно се прописују даље мере рехабилитације, чија је сврха обнављање нормалне крвне слике, стабилизација кардиоваскуларне активности, нормализација неуролошког статуса. Обавезно се практикује довољна психолошка подршка.
Хируршко лечење
Операција се изводи како би се што више уклонио фокус тумора, што заузврат треба да смањи интракранијални притисак, смањи неуролошку инсуфицијенцију и обезбеди неопходан биоматеријал за истраживање.
- Операција се изводи у специјализованом неурохируршком одељењу или клиници чији стручњаци имају искуства у неуро-онколошким интервенцијама.
- Хирург врши приступ пластичном трепанацијом костију у подручју сумње на локализацију глиома.
- Ако се неоплазма налази анатомски близу моторних подручја или путева, или у језгрима или дуж кранијалних живаца, користи се интраоперативни неурофизиолошки мониторинг.
- Неуронавигациони системи, интраоперативна флуоресцентна навигација са 5-аминолевуленском киселином је пожељна за максимизирање уклањања неоплазме.
- Након интервенције, контролни ЦТ или МРИ (са или без убризгавања контраста) се врши 1-2 дана.
Ако је хируршка ресекција глиома немогућа или је у почетку препозната као нецелесообразна, или ако се сумња на лимфом централног нервног система, врши се биопсија (отворена, стереотактичка, са навигационим праћењем итд.). |
Пацијенти са церебралном глиоматозом се верификују стереотактичком биопсијом, јер терапијска тактика у великој мери зависи од хистолошке слике. |
У одређеним ситуацијама - код старијих пацијената, у случају тешких неуролошких поремећаја, у случају локализације глиома у трупу и другим виталним деловима - лечење се планира на основу симптома и информација са снимања након опште медицинске консултације. |
Пацијентима са пилоидним астроцитомом, као и нодуларним облицима неоплазми можданог стабла и егзофитским процесима, препоручује се ресекција или отворена биопсија. |
Пацијенти са дифузним понтинским глиомом и другим дифузним неоплазмама трупа лече се зрачењем и терапијом антитуморским лековима. Верификација у таквим случајевима није потребна. |
Пацијенти са квадриплегичним плочастим глиомом након уклањања церебралне хидроцеле подвргавају се систематској магнетној резонанцији и клиничком праћењу. Ако неоплазма показује знаке раста, уклања се даљим зрачењем. |
Када се изврши парцијална ресекција или биопсија нискостепеног малигног глиома, пацијенти са два или више фактора ризика нужно се лече зрачењем и/или хемотерапијом. |
Тотална ресекција је обавезна за пацијенте са субепендималним гигантским ћелијским астроцитомом. |
Еверолимус се прописује за дифузни субепендимал џиновски ћелијски астроцитом. |
Пилоидни астроцитом треба уклонити магнетном резонанцом након интервенције како би се разјаснио квалитет радикалне ресекције туморског ткива. |
Код глиобластома, постоперативну терапију треба комбиновати (зрачење + хемотерапија) са применом темозоломида. |
Код анапластичног астроцитома након операције, индицирана је радиотерапија са даљом терапијом лековима. Користе се ломустин, темозоломид. |
Пацијенти са анапластичним олигодендроглиомом или олигоастроцитомом примају и зрачење и хемотерапију (монотерапију темозоломидом или PCV) након операције. |
Старији пацијенти са екстензивним високомалигним глиомом се зраче у хипофракционисаном режиму или се спроводи монотерапија темозоломидом. |
У случају рецидива глиома, могућност реоперације и накнадне тактике лечења разматра конзилијум специјалиста. Оптимални режим за рецидиве: реоперација + системска хемотерапија + поновљено излагање зрачењу + палијативне мере. Уколико постоје локализована мања подручја рекурентног раста тумора, може се користити радиохирургија. |
Лекови избора за рекурентни раст глиома су Темозоломид и Бевацизумаб. |
Рецидив високо малигних олигодендроглиома и анапластичних астроцитома је индикација за лечење темозоломидом. |
Плеоморфни ксантоастроцитом се уклања без обавезне адјувантне хемотерапије. |
Једна од особености глиома је тешкоћа у њиховом лечењу и уклањању. Хирург има за циљ да што потпуније уклони ткива неоплазме, како би постигао компензацију стања. Многи пацијенти су у стању да побољшају квалитет живота и продуже га, али за високо малигне туморе прогноза остаје неповољна: постоји повећана вероватноћа поновног раста патолошког фокуса.
Исхрана за глиом мозга
Дијета за пацијенте са малигним туморима - важна тачка, којој, нажалост, многи људи не обраћају много пажње. У међувремену, захваљујући променама у исхрани, могуће је успорити развој глиома и ојачати и пољуљани имунитет.
Главне области промене исхране:
- Нормализација метаболичких процеса, јачање имунолошке заштите;
- Детоксикација тела;
- Оптимизација енергетског потенцијала;
- Обезбеђивање нормалног функционисања свих органа и система тела током тако тешког периода за њих.
Рационална и уравнотежена исхрана је неопходна, како код пацијената са раним стадијумима малигних неоплазми ниског интензитета, тако и код пацијената са последњом фазом глиобластома. Пажљиво одабрана исхрана доприноси побољшању општег благостања, опоравку оштећених ткива, што је посебно важно на позадини цитостатског и радиотерапијског третмана. Равнотежа нутритивних компоненти и правилни метаболички процеси спречавају стварање инфективних жаришта, блокирају инфламаторне реакције, спречавају исцрпљивање организма.
Следећа храна и пића се препоручују за глиом мозга:
- Црвено, жуто и наранџасто воће и поврће (парадајз, брескве, кајсије, шаргарепа, цвекла, агруми) које садрже каротеноиде, који штите здраве ћелије од негативних ефеката радиотерапије;
- Купус (карфиол, броколи, прокулица), ротквица, сенф и други биљни производи који садрже индол - активну супстанцу која неутралише неповољне токсичне и хемијске факторе;
- Зеленило (копар, першун, млади листови маслачка и коприве, рабарбара, рукола, спанаћ), зелени грашак и шпаргле, пасуљ шпаргле и алге (морске алге, спирулина, хлорела);
- Зелени чај;
- Бели лук, црни лук, ананас, који имају антитуморска и детоксикациона својства;
- Мекиње, житарице, хлеб од целог зрна, проклијале клице махунарки, житарице и семенке;
- Тамно грожђе, малине, јагоде и јагоде, боровнице, купине, нар, рибизле, црне рибизле, јаворовина, боровнице, морски кркавац, трешње и друге бобице које садрже природне антиоксиданте који смањују негативне ефекте слободних радикала, вируса и канцерогена;
- Млечни производи са ниским садржајем масти.
Не треба оптерећивати систем за варење и цело тело тешком и масном храном. Корисно је користити свеже цеђене домаће сокове, смутије, грицкалице. У јела треба додавати изворе омега-3 масних киселина, као што су рибље уље, уље од ланеног семена или семе лана.
Боље је потпуно избегавати шећер и слаткише. Али кашика меда са шољом воде неће шкодити: пчелињи производи имају изражено антиинфламаторно, антиоксидативно и антитуморско дејство. Једина контраиндикација за употребу меда је алергија на производ.
Из исхране треба искључити:
- Месо, маст, изнутрице;
- Путер, масни млечни производи;
- Димљено месо, кобасице, конзервирано месо и риба;
- Алкохол у било ком облику;
- Слаткиши, пецива, торте и пецива, бомбоне и чоколаде;
- Готова храна, брза храна, грицкалице;
- Пржена храна.
Требало би да конзумирате довољно поврћа, зеленила, воћа и чисте воде за пиће свакодневно.
Током хемотерапије и неко време након ње, треба пити домаће сокове од поврћа и воћа, јести домаћи немасни свјежи сир, млеко и сир. Важно је пити доста течности, прати зубе и често испирати уста (око 4 пута дневно).
Оптимални оброци за пацијенте са глиомом мозга:
- Поврћне чорбе;
- Прилози и супе од житарица (пожељно хељда, овсена каша, пиринач, кускус, булгур);
- Парени колачи од сира, пудинзи, чорбе;
- Динстано и печено поврће;
- Гулаши, повртне супе, прва и друга јела од махунарки (укључујући соју), паштете и суфле;
- Смутији, зелени чај, компоти и грицкалице.
Превенција
Ако особа води здрав начин живота, а међу његовим рођацима није било случајева онкопатологије, има све шансе да не добије глиом мозга. Не постоји специфична превенција таквих тумора, па се главне превентивне тачке сматрају правилном исхраном, физичком активношћу, избегавањем лоших навика, одсуством професионалних и кућних опасности.
Стручњаци дају неколико једноставних, али ефикасних препорука:
- Пијте више чисте воде, избегавајте заслађене газиране напитке, паковане сокове, енергетска пића и алкохол.
- Избегавајте опасности на послу и у домаћинству: мање контакта са хемикалијама, корозивним растворима и течностима.
- Покушајте да припремате храну кувањем, динстањем, печењем, али не и пржењем. Дајте предност здравим, квалитетним домаћим намирницама.
- Велики део ваше исхране треба да чини биљна храна, укључујући и зелено поврће, без обзира на доба године.
- Још један негативан фактор је прекомерна тежина, које се треба решити. Контрола тежине је веома важна за здравље целог тела.
- Биљна уља треба увек имати предност у односу на путер и маст.
- Ако је могуће, пожељно је дати предност еколошки прихватљивим производима, месу без хормона, поврћу и воћу без нитрата и пестицида. Боље је потпуно избегавати црвено месо.
- Не узимајте мултивитаминске препарате без индикација и у великим количинама. Не узимајте никакве лекове без лекарског рецепта: самолечење је често веома, веома опасно.
- Уколико се појаве сумњиви симптоми, потребно је посетити лекара, не чекајући погоршање ситуације, развој нежељених ефеката и компликација.
- Слаткиши и храна са високим гликемијским индексом су непожељна компонента исхране.
- Што раније особа оде код лекара, веће су јој шансе за излечење (а то се односи на скоро сваку болест, укључујући и глиом мозга).
Да бисте спречили стварање онкопатологије, потребно је довољно времена за спавање и одмор, избегавати прекомерну конзумацију алкохолних пића, дати предност квалитетној природној храни, смањити употребу гаџета (посебно мобилних телефона).
Туморске болести се често јављају код старијих и старијих особа. Стога је важно пратити сопствено здравље од малих ногу и не изазивати патолошке процесе нездравим начином живота и нездравим навикама.
Тачни узроци онкологије још увек нису разјашњени. Међутим, одређену улогу, наравно, играју неповољни услови професионалног и животне средине, изложеност јонизујућем и електромагнетном зрачењу, хормонске промене. Немојте дуго и редовно остајати под сунцем, дозволити нагле промене температуре околине, прегревати се у кади или сауни, често се купати у топлим купкама или тушевима.
Још једно питање: како спречити поновну појаву глиома мозга након успешног лечења? Поновна појава раста неоплазме је сложена и, нажалост, честа компликација, коју је тешко унапред предвидети. Пацијентима се може препоручити да се редовно подвргавају превентивним прегледима и контролама, да посећују онколога и лекара најмање два пута годишње, да воде здрав начин живота, да једу здраву и природну храну, да се баве умереном физичком активношћу. Још један услов је љубав према животу, здрав оптимизам, позитиван став према успеху под било којим околностима. Ово такође укључује пријатељску атмосферу у породици и на послу, стрпљење и безусловну подршку блиских људи.
Прогноза
Стање мозга и карактеристике глиома у време његовог откривања утичу на стопу преживљавања колико и примењени третман. Задовољавајуће опште здравствено стање пацијента и његове године побољшавају прогнозу (прогноза је оптимистичнија код младих пацијената). Важан показатељ је хистолошка слика неоплазме. Дакле, глиоми ниског степена имају бољу прогнозу од анапластичних глиома, а још више од глиобластома (најнеповољнијих туморских процеса). Астроцитоми имају лошију прогнозу од олигодендроглиома.
Малигни астроцитоми слабо реагују на терапију и имају релативно ниску стопу преживљавања од шест до пет година. Истовремено, очекивани животни век код глиома ниског степена процењује се на 1-10 година.
Малигни астроцитоми су у суштини неизлечиви. Правац лечења обично подразумева смањење неуролошких манифестација (укључујући когнитивну дисфункцију) и повећање животног века уз одржавање највишег могућег квалитета живота. Симптоматска терапија се привлачи на позадини рехабилитационих мера. Рад психолога је такође важан.
Током протекле деценије, научници су постигли известан напредак у разумевању природе тумора мозга и начина њиховог лечења. Много више треба учинити како би се оптимизовала прогноза болести. Примарни задатак специјалиста данас је следећи: глиом мозга треба да има неколико шема за ефикасно отклањање проблема одједном, како у раним тако и у каснијим фазама развоја.

